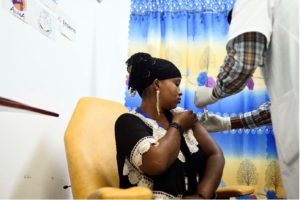
Des résultats prometteurs concernant la sûreté et la réponse immunitaire induite par la vaccination contre Ebola
|
|
© Inserm/Patrick Delapierre, 2018
Des épidémies de maladies à virus Ebola surviennent périodiquement dans plusieurs pays d’Afrique sub-saharienne. Si des vaccins existent et ont déjà reçu une préqualification[1] de l’OMS contre l’espèce Ebolavirus Zaïre, il est essentiel de poursuivre et d’intensifier les efforts afin d’approfondir les données disponibles, pour développer une stratégie de vaccination sûre et efficace contre le virus Ebola, chez les adultes comme chez les enfants. Le consortium international PREVAC, qui inclut des scientifiques de l’Inserm et d’institutions africaines, américaines et britanniques, publie dans le New England Journal of Medicine les résultats d’un large essai clinique randomisé en Afrique de l’Ouest. Ceux-ci confirment la sûreté de trois schémas vaccinaux différents, ainsi que le maintien à 12 mois de la réponse immunitaire induite.
Dans un contexte où de nombreux pays d’Afrique subsaharienne font régulièrement face à des flambées épidémiques de la maladie d’Ebola, les vaccins sont plus que jamais considérés comme un outil central pour lutter contre sa propagation.
Depuis 2019, deux vaccins ont obtenu une préqualification de l’OMS contre l’espèce Ebolavirus Zaïre : le vaccin rVSVΔG-ZEBOV-GP, développé par Merck, Sharpe & Dohme, Corp., et la stratégie vaccinale comprenant les vaccins Ad26.ZEBOV et MVA-BN-Filo de Janssen Vaccines & Prevention, BV.
Au-delà de ces avancées, la recherche sur ces vaccins continue. En effet, il est nécessaire d’obtenir des données complémentaires pour établir leurs recommandations d’utilisation, notamment pour les différentes catégories de personnes susceptibles de les recevoir.
Trois schémas vaccinaux testés
C’est tout l’objectif du consortium international PREVAC. Débuté en 2017, un vaste un essai de phase 2 multicentrique, randomisé et contrôlé contre placebo a mobilisé des équipes de recherche africaines, européennes et américaines, travaillant ensemble au Libéria, en Guinée, en Sierra Leone et au Mali. À ce jour, il s’agit de l’un des essais les plus importants sur la vaccination contre le virus Ebola – à la fois chez des adultes et chez des enfants d’un an et plus.
L’essai visait à mesurer la rapidité, l’intensité et la durée des réponses immunitaires générées par trois différents schémas vaccinaux contre le virus Ebola, impliquant les vaccins évoqués plus haut. Il consistait également à évaluer l’innocuité et la tolérance des différents produits administrés.
- Le premier schéma vaccinal testé consistait à injecter une dose du vaccin ZEBOV suivie 56 jours plus tard d’une dose de MVA-BN-Filo;
- Le deuxième schéma consistait à injecter une dose de rVSVΔG-ZEBOV-GP ;
- Enfin le troisième schéma commençait par une dose de rVSVΔG-ZEBOV-GP suivie 56 jours après d’un rappel avec ce même vaccin.
Au total, l’essai a porté sur 1 400 adultes et 1 401 enfants âgés de 1 à 17 ans, qui ont été répartis en plusieurs groupes afin de tester et de comparer les trois schémas vaccinaux contre placebo.
Les données obtenues suggèrent que les trois schémas vaccinaux sont sûrs et bien tolérés chez les adultes et les enfants. Après la vaccination et dans les sept jours qui suivent, la majorité des participants rapportent des douleurs au point d’injection et d’autres symptômes sans gravité (fièvre, douleurs musculaires et articulaires, maux de tête…), qui disparaissent généralement au bout de sept jours.
Concernant la réponse immunitaire, les trois schémas vaccinaux ont permis une augmentation rapide, au bout de 14 jours, de la quantité d’anticorps dirigés contre le virus, avec un pic entre 1 et 3 mois après la première vaccination. S’il n’est pas possible d’affirmer que cette réponse immunitaire permet de prévenir l’infection, la littérature scientifique suggère qu’il existe une corrélation forte entre la quantité de ces anticorps et la protection contre le virus.
Cette quantité d’anticorps demeure détectable jusqu’à 12 mois après la première injection. Il est par ailleurs intéressant de constater que cette réponse immunitaire induite par la vaccination est plus élevée chez les enfants que chez les adultes.
« Les données collectées lors de cet essai clinique sont précieuses car elles permettent de confirmer la sécurité et l’efficacité potentielle des vaccins disponibles, ce qui va permettre d’affiner les recommandations de vaccination en période d’épidémie d’Ebolavirus Zaïre mais aussi en période inter-épidémies, chez les populations à risque », précise Yazdan Yazdanpanah, co-investigateur principal de l’essai, chercheur Inserm et directeur de l’ANRS | Maladies infectieuses émergentes.
« Cet essai est marqué par un fort taux de rétention des participants grâce à l’implication sans faille de tous les professionnels sur le terrain à et l’adhésion de la population à la recherche qui a permis d’aboutir à ces résultats », explique Mark Kieh, co-investigateur principal de l’essai.
« L’essai PREVAC est un véritable exemple de succès pour la recherche internationale. Nous montrons qu’avec une solide collaboration en nous appuyant sur des partenariats robustes, nous faisons avancer la recherche contre Ebola, dans les régions du monde les plus touchées par la maladie », souligne H. Clifford Lane, directeur adjoint du National Institute of Allergy and Infectious Diseases (NIAID) pour la recherche clinique et les projets spéciaux.
Les travaux du consortium PREVAC en Afrique de l’Ouest se poursuivent grâce à un financement européen de l’European & Developing Countries Clinical Trials Partnership (EDCTP) soutenu par l’Union européenne. Les participants sont désormais suivis pendant une durée de 5 ans pour évaluer leur sécurité à long terme et la durabilité de la réponse immunitaire. Il est crucial d’obtenir de telles données, qui apporteront des informations sur la nécessité de faire un rappel ou non à des personnes déjà vaccinées.

À propos de PREVAC
PREVAC (Partnership for Research on Ebola Vaccinations ou Partenariat pour la recherche sur la vaccination contre Ebola) est un consortium international qui mène des recherches en Afrique de l’Ouest pour évaluer la sécurité et l’efficacité de la vaccination contre Ebola.
Le projet bénéficie d’un cofinancement de l’Inserm, du NIAID, de la London School of Hygiene & Tropical Medicine (LSHTM) et du College of Medicine and Allied Health Sciences (Comahs), ainsi que d’un soutien de la Guinée, du Liberia, du Mali et de la Sierra Leone. Le soutien sur le terrain de l’ONG Alima a également été crucial pour favoriser l’adhésion de la population à la recherche et le suivi des volontaires. Les industriels Merck et Johnson & Johnson ont fourni les vaccins utilisés dans le cadre de l’essai.
Le projet a aussi bénéficié d’un financement supplémentaire pour continuer le suivi des volontaires sur le long terme (projet PREVAC-up coordonné par l’Inserm) via le programme EDCTP2 (European and Developing Countries Clinical Trials Partnership) soutenu par l’Union européenne.
Organisations partenaires de PREVAC-up
Institut national de la santé et de la recherche médicale (Inserm)*, France ; Vaccine Research Institute (VRI), France ; Centre national de formation et de recherche en santé rurale (CNFRSR)*, Guinée ; Institut Bouisson-Bertrand* (IBB) / Centre de recherche et de formation en infectiologie (CERFIG) France/Guinée ; London School of Hygiene and Tropical Medicine (LSHTM)*, Royaume-Uni ; University of Sierra Leone, College of Medicine and Allied Health Sciences (Comahs)*, Sierra Leone ; Alliance for International Medical Action (ALIMA)*, France ; Inserm-Transfert SA*, France ; National Institute of Allergy and Infectious Diseases (NIAID), États-Unis ; Université des sciences, des techniques et des technologies de Bamako (USTTB)*, Mali ; Ministry of Health (Centre pour le développement des vaccins – Mali)*, Mali ; National Public Health Institute of Liberia (NPHIL), Libéria *Signataires de la convention de subvention de l’EDCTP Inserm’s participation in PREVAC is in part through a subcontract with Leidos Biomedical Research, Inc. which operates the Frederick National Laboratory for Cancer Research on behalf of the National Cancer Institute. The content of this publication does not necessarily reflect the views or policies of the Department of Health and Human Services, nor does mention of trade names, commercial products, or organizations imply endorsement by the U.S. government. The PREVAC-UP project is funded by the European and Developing Countries Clinical Trials Partnership (EDCTP2) programme supported by the European Union and the UK Department of Health & Social Care (Grant number RIA2017S – 2014 -PREVAC-UP). Besides the EDCTP2 grant, PREVAC-UP benefits from co-funding from Inserm, the NIAID, the LSHTM and the COMAHS as well as host country support from Liberia, Sierra Leone, Guinea and Mali. |
Sources
Vaccines for Ebola virus disease: the PREVAC randomized trial
Mark Kieh *1 M.D., M.S.M.H.C., Laura Richert*2 M.D., Ph.D., Abdoul Habib Beavogui3 M.D., Ph.D., Birgit Grund20 Ph.D., Bailah Leigh5 M.D., M.Sc., Eric D’Ortenzio6,7,8 M.D., Seydou Doumbia9 M.D., Ph.D., Edouard Lhomme2 M.D., Ph.D., Samba Sow10 M.D., Renaud Vatrinet6 Ph.D., Céline Roy11 Ph.D, Stephen B. Kennedy1 M.D., M.Sc., Sylvain Faye12 Ph.D., Shelley Lees13 Ph.D., Niouma Pascal Millimouno14 M.D., Alseny Modet Camara14 M.D, Mohamed Samai5 M.B.B.S., Ph.D., Gibrilla F Deen5 M.D., M.Sc., Moussa Doumbia15 M.D., Hélène Espérou6 M.D., Jerome Pierson16 Ph.D., Deborah Watson-Jones13 M.D., Ph.D, Alpha Diallo6,8 M.D., M.P.H., Deborah Wentworth4 M.P.H., Chelsea McLean17 Ph.D., Jakub Simon18 M.D., Aurélie Wiedemann6, 19 Ph.D., Bonnie Dighero-Kemp16 B.Sc., Lisa Hensley16 Ph.D., M.S.P.H., H. Clifford Lane16 M.D., Yves Levy6,19 M.D., Ph.D., Peter Piot13 M.D., Ph.D., Brian Greenwood13 M.D., Geneviève Chêne11 M.D., Ph.D., James Neaton*4 Ph.D., Yazdan Yazdanpanah*6,7,8 M.D., Ph.D.
*Contributed equally
- Partnership for Research on Ebola Virus in Liberia (PREVAIL), Monrovia, Liberia
- Univ. Bordeaux, INSERM, Institut Bergonié, CHU de Bordeaux, CIC-EC 1401, Euclid/F-CRIN clinical trials platform and U1219 BPH, Inria, Sistm, F-33000 Bordeaux, France
- Centre National de Formation et de Recherche en Santé Rurale de Maferinyah, Maferinyah, Guinea
- School of Public Health, University of Minnesota, Minneapolis, MN, USA
- College of Medicine and Allied Health Sciences (COMAHS), University of Sierra Leone, Freetown, Sierra Leone
- French Institute for Health and Medical Research (INSERM), 75013 Paris, France
- AP-HP, Hôpital Bichat-Claude Bernard, Service de Maladies Infectieuses et Tropicales, Paris F-75018, France
- ANRS|Emerging Infectious Diseases (France Recherche Nord&Sud Sida-hiv Hépatites|Emerging Infectious Diseases), Paris, France
- University Clinical Research Center (UCRC), University of Sciences, Techniques and Technologies of Bamako (USTTB), Bamako, Mali
- Center for Vaccine Development and Global Health, University of Maryland School
- Univ. Bordeaux, INSERM, Institut Bergonié, CHU de Bordeaux, CIC-EC 1401, Euclid/F-CRIN clinical trials platform, F-33000 Bordeaux, France
- Département de Sociologie, FLSH, Université Cheikh Anta DIOP, Dakar, Sénégal
- London School of Hygiene & Tropical Medicine, London, UK
- The Alliance for International Medical Action, Alima, B.P.15530 Dakar, Sénégal
- Centre pour le Développement des Vaccins, Ministère de la Santé, Bamako, Mali
- National Institute of Allergy and Infectious Diseases, Bethesda, MD, USA or under contract/subcontract to NIAID
- Janssen Vaccines and Prevention BV Leiden, The Netherlands
- Merck Sharp & Dohme Corp., Inc., Kenilworth, NJ, USA
- Vaccine Research Institute, Univ. Paris Est Créteil, Henri Mondor Hospital, Créteil, France
- School of Statistics, University of Minnesota, Minneapolis, MN, USA
NEJM, décembre 2022
DOI : 10.1056/NEJMoa2200072
Contact presse
Accéder à la salle de presse de l’Inserm
[1] La préqualification signifie qu’un vaccin satisfait aux normes de qualité, d’innocuité et d’efficacité de l’OMS. Sur la base de cette recommandation, les organismes du système des Nations unies et l’Alliance Gavi peuvent acheter le vaccin pour les pays à risque.